Gluconeogénesis
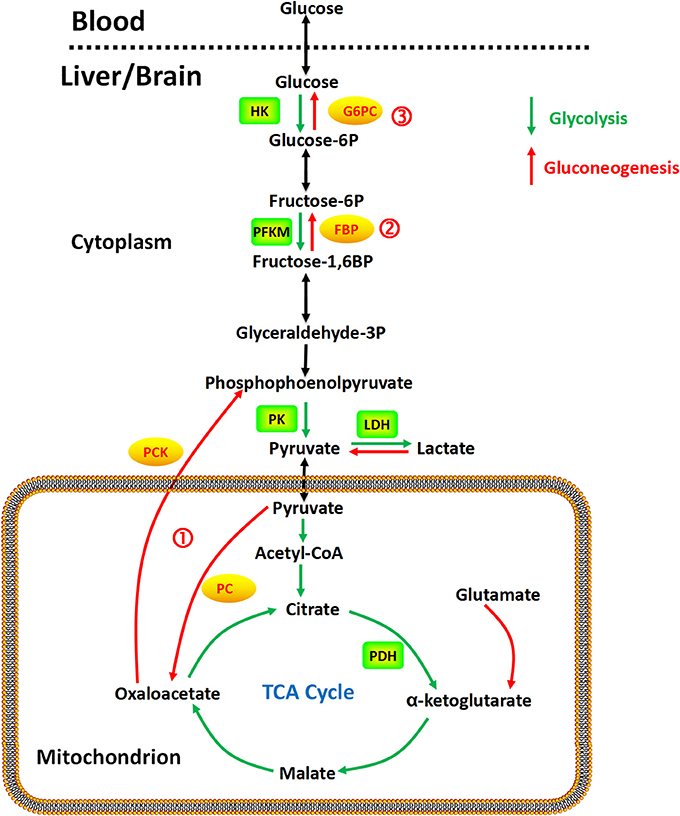
Este documento se enfoca en la gluconeogénesis y sus enzimas clave asociadas, junto con anticuerpos relevantes y referencias de investigación. Explica las funciones de múltiples enzimas involucradas en la gluconeogénesis y la glucólisis, como las isoformas de enolasa (ENO1/2/3), la fructosa-1,6-bisfosfatasa 1 (FBP1), la glucosa-6-fosfato isomerasa (GPI), la fosfoenolpiruvato carboxiquinasa (PCK1/2), la fosfoglicerato mutasa 1 (PGAM1), la fosfoglicerato quinasa 1 (PGK1) y la piruvato carboxilasa (PC). Estas enzimas desempeñan roles cruciales en los procesos metabólicos, y su expresión anormal está relacionada con la progresión tumoral (por ejemplo, cáncer de mama, cáncer de pulmón, carcinoma renal de células claras) y otras enfermedades. Además, el documento presenta un diagrama regulador del metabolismo de la glucosa (que abarca la glucólisis, la gluconeogénesis y el ciclo de los ácidos tricarboxílicos) y proporciona información detallada sobre anticuerpos específicos dirigidos a las enzimas mencionadas, incluidos sus números de catálogo, reactividades y aplicaciones. También se incluyen referencias de investigación relevantes para respaldar los hallazgos discutidos.
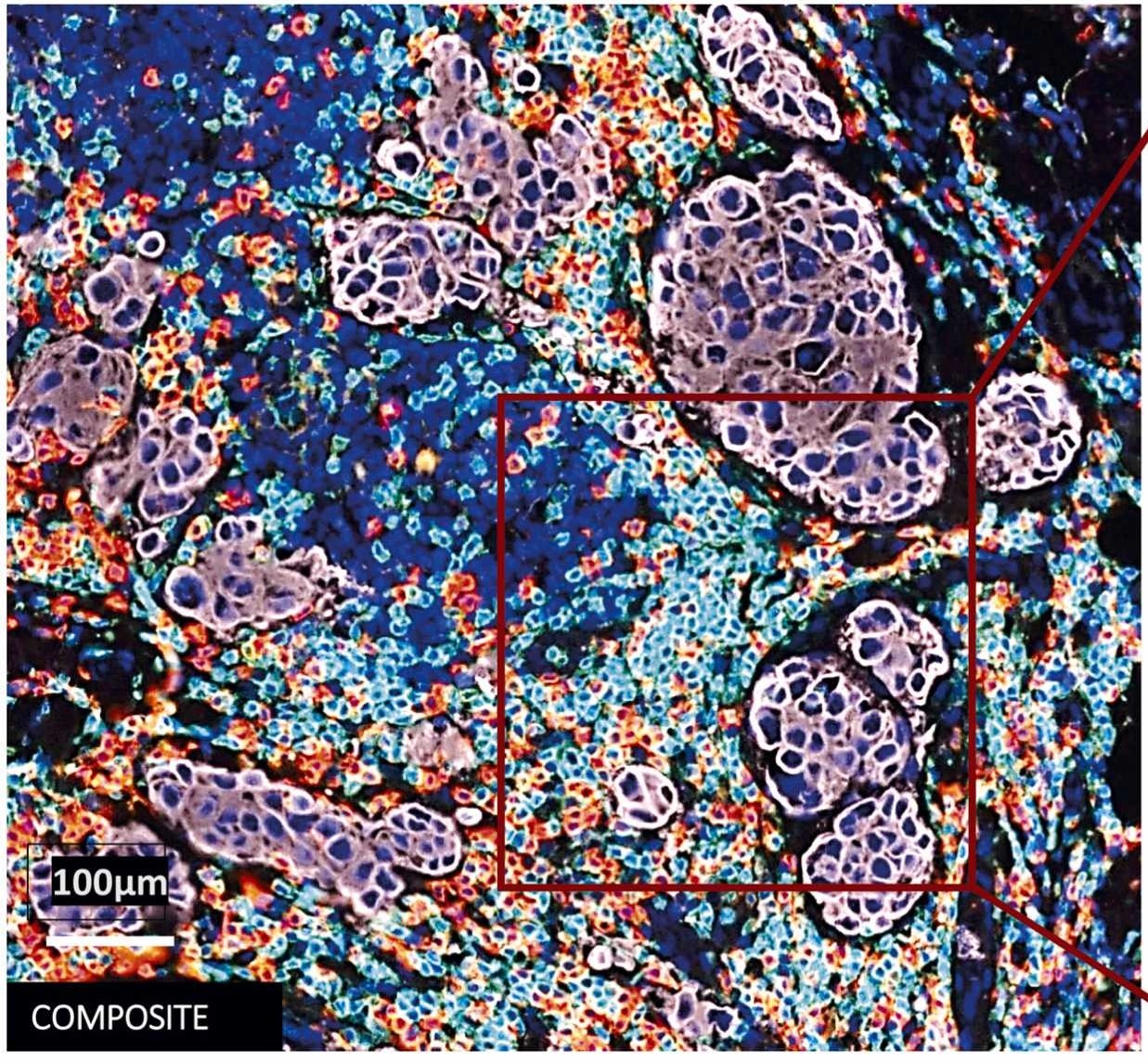
Compartir Literatura: Inmunofluorescencia Múltiple para el Análisis Inmune de Tejido Tumoral e Investigación de Distribución Espacial Celular
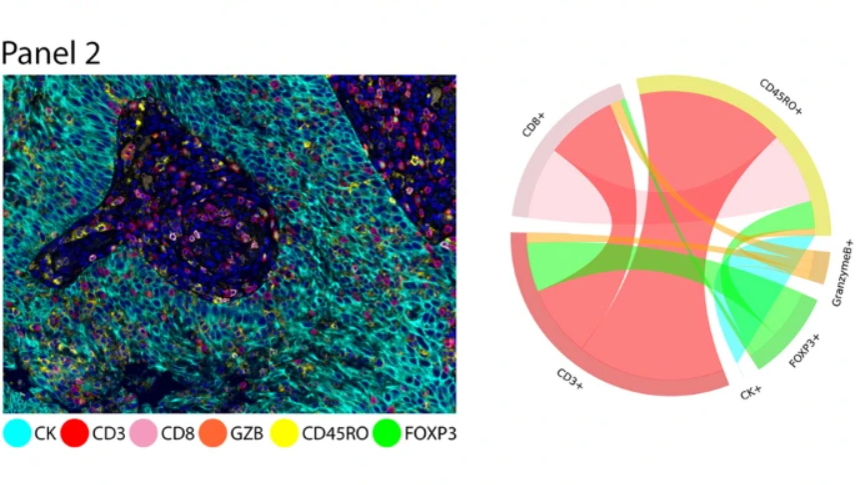
Aunque la inmunoterapia tumoral se ha desarrollado rápidamente y ha logrado resultados significativos, los tumores malignos pueden escapar de la vigilancia inmunitaria al construir un microambiente inmunosupresor, lo que limita severamente la eficacia del tratamiento. Tras el descubrimiento de moléculas de puntos de control inmunológico como PD-1 y CTLA-4 y sus roles en la evasión inmunitaria tumoral, aclarar la interacción entre las células inmunológicas y las células cancerosas se ha convertido en un prerrequisito fundamental para el desarrollo de nuevas inmunoterapias. La inmunofluorescencia múltiple (mIF) es un método fiable de alto rendimiento que puede observar directamente múltiples biomarcadores expresados por células individuales y analizar las relaciones espaciales de estos biomarcadores en diferentes poblaciones celulares, lo que es imposible con las técnicas tradicionales de inmunohistoquímica (IHC). Por lo tanto, el estudio "Immuno-profiling and cellular spatial analysis using five immune oncology multiplex immunofluorescence panels for paraffin tumor tissue" puede identificar múltiples subpoblaciones celulares mediante la combinación de anticuerpos cuidadosamente seleccionados. El protocolo manual de amplificación de señal de tiramida (TSA) se utilizó como referencia estándar para validar la tinción múltiple. La tinción automatizada redujo significativamente el tiempo original de tinción manual de 4-5 días a 14-17 horas, al mismo tiempo que mejoró la consistencia de la tinción. La literatura demuestra el proceso de optimización y la reproducibilidad de la tinción TSA automatizada, y valida su valor de aplicación en la investigación del microambiente tumoral y el análisis de la distribución espacial del fenotipo celular en una cohorte pequeña de muestras de cáncer de pulmón no de células pequeñas (CPNPC).
Compartir Literatura: Evaluación de la Infiltración de Células Inflamatorias en Biopsias de Trasplante Renal mediante Tecnología de Inmunofluorescencia Múltiple
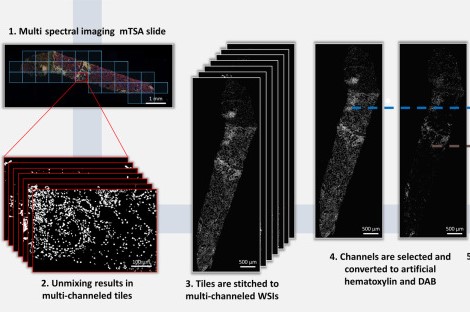
La función retardada del injerto (FRI) después del trasplante renal es una complicación común, definida como la necesidad de diálisis dentro de los 7 días posteriores al trasplante, y es un importante factor de riesgo para la lesión renal crónica trasplantada. La fibrosis intersticial y la atrofia tubular (FIAT) son manifestaciones típicas de la lesión renal crónica. Sin embargo, no todos los pacientes con FRI progresan a FIAT, y la compleja asociación entre ellas sigue sin estar clara. El principal cuello de botella es que los métodos de evaluación tradicionales tienen dificultades para cuantificar con precisión las características de la infiltración inflamatoria y no pueden identificar tempranamente los marcadores predictivos de la progresión de la FIAT. La evaluación histológica tradicional depende del juicio subjetivo de los patólogos, con una precisión muy influenciada por la experiencia, y no puede capturar simultáneamente información sobre el fenotipo, la densidad y la distribución espacial de múltiples tipos de células inmunes, lo que limita la exploración en profundidad de la asociación entre el microambiente inflamatorio y el pronóstico del injerto. "Evaluación cuantitativa de los infiltrados inflamatorios en biopsias de trasplante renal mediante amplificación de señal de ti ramida múltiple y aprendizaje profundo" se centra en la innovación tecnológica en la evaluación cuantitativa de la infiltración inflamatoria en biopsias de trasplante renal, con el objetivo de resolver el reto clínico de predecir la progresión de la fibrosis intersticial y la atrofia tubular en pacientes con función retardada del injerto, y lograr un análisis cuantitativo preciso de la infiltración inflamatoria a través de la integración tecnológica.
Revisión de Literatura: Avances Prácticos en Técnicas de Inmunohistoquímica y Inmunofluorescencia Multiplex
En los últimos años, el análisis del complejo paisaje inmunológico del microambiente tumoral (TME) se ha convertido en el núcleo de la investigación en oncología de precisión. Sin embargo, la práctica clínica rutinaria sigue dependiendo de la tinción H&E y la detección de IHQ cromogénica de un solo marcador, lo que presenta limitaciones como el desperdicio de tejido, la inability de evaluar múltiples marcadores simultáneamente y la no idoneidad para el análisis cuantitativo y espacial, lo que dificulta satisfacer las necesidades de la investigación del microambiente tumoral y la predicción de la respuesta a la inmunoterapia. La abundancia celular y la disposición espacial del microambiente tumoral afectan la progresión tumoral y la respuesta al tratamiento. Al usar IHQ única para evaluar la expresión de PD-L1 y predecir la respuesta a la inmunoterapia, existen problemas como una reproducibilidad deficiente, la inability de identificar claramente el tipo celular de expresión y la dificultad para cuantificar la disposición espacial. La tinción múltiple, que puede dirigirse simultáneamente a múltiples proteínas a través de tinción fluorescente o cromogénica, puede caracterizar el perfil de coexpresión y la disposición espacial de los marcadores, mostrando un rendimiento superior a los métodos de detección múltiple en la predicción de la respuesta a la inmunoterapia. Tiene un amplio valor de aplicación en la investigación del microambiente tumoral, el análisis de heterogeneidad espacial de biomarcadores, la resolución del problema de detección de múltiples marcadores en muestras pequeñas y la estratificación de pacientes en ensayos clínicos. Con la continuada optimización y la disminución de la dificultad de implementación, es más adecuada para el uso clínico rutinario. "Multiplex Immunohistochemistry and Immunofluorescence: A Practical Update for Pathologists" es un artículo de revisión para patólogos, centrado en las técnicas de inmunohistoquímica múltiple (mIHC) e inmunofluorescencia múltiple (mIF). Al detectar simultáneamente múltiples biomarcadores en la misma sección, mejora en gran medida el contenido informativo y la precisión del diagnóstico patológico. Actualmente, los enfoques técnicos para lograr la detección múltiple incluyen principalmente IHC/mIF múltiple basada en TSA y otros métodos, imágenes de espectrometría de masas y perfilado espacial digital (DSP), y tinción múltiple virtual lograda a través del registro de secciones consecutivas. Aunque estas técnicas aún enfrentan desafíos en los procedimientos estandarizados y el análisis de datos, con la madurez de la tecnología de patología digital, la tinción múltiple ha ido ganando viabilidad para la traducción clínica y se espera que se convierta en un método rutinario para guiar las decisiones de inmunoterapia tumoral en un futuro cercano.
Compartir Literatura: Explorar las Características de Expresión de STING en el Cáncer Colorrectal Utilizando Fluorescencia Múltiple
STING exhibe características de expresión en múltiples tipos de células en tejidos cancerosos, incluidos linfocitos, células asesinas naturales, células endoteliales y células epiteliales. Los estudios actuales sobre la expresión de STING en el campo del cáncer se basan principalmente en niveles de ARN, lo que dificulta distinguir las diferencias de expresión específicas de las células, y el significado clínico de STING en las células tumorales y las células inflamatorias asociadas al tumor aún no está completamente claro. Sobre la base de esto, un artículo de investigación publicado en Pathology titulado "High-level STING expression in tumour and inflammatory cells is linked to microsatellite instability and favourable tumour parameters in a cohort of over 1,900 colorectal cancer patients" utilizó tecnología de inmunohistoquímica fluorescente múltiple (mIHC) para analizar cuantitativamente la expresión de STING en diferentes tipos de células en el cáncer colorrectal y explorar su asociación con las características clinicopatológicas. Esto proporciona una base importante para el estudio de los mecanismos inmunitarios y la exploración de posibles dianas terapéuticas en el cáncer colorrectal.
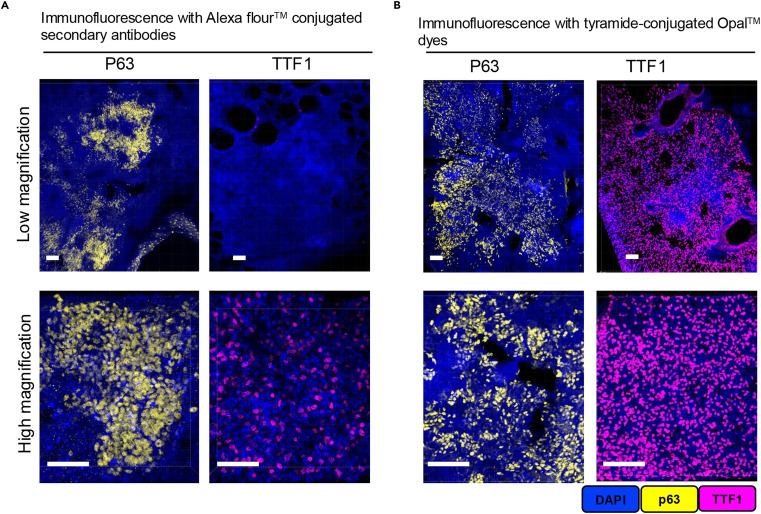
Compartir literatura: Tinción fluorescente multiplexada de lesiones de tuberculosis pulmonar basada en TSA
El principio fundamental de la tecnología TSA es que los anticuerpos secundarios conjugados con peroxidasa de rábano picante (HRP), en presencia de peróxido de hidrógeno, catalizan la conversión de las tiramidas marcadas fluorescentemente en formas activas, que luego se unen covalentemente a los residuos de tirosina cerca de los antígenos diana, logrando una amplificación en cascada de las señales. El estudio seleccionó los colorantes fluorescentes Opal como etiquetas, que, en comparación con los anticuerpos secundarios fluorescentes tradicionales, mejoran significativamente la sensibilidad de la señal y permiten la imagenología con potencia láser baja, reduciendo el fotoblanching tisular.
Compartir literatura: Análisis de inmunofluorescencia múltiple del cáncer de mama triple negativo temprano
Estudios anteriores han demostrado que la terapia de mantenimiento con ciclofosfamida-metotrexato (CM) no reduce significativamente el riesgo de recurrencia en pacientes con cáncer de mama triple negativo (TNBC) de manera estadísticamente significativa. Sin embargo, los pacientes con niveles altos de linfocitos infiltrantes tumorales estromales (sTILs, >500) experimentaron una reducción más pronunciada en el riesgo de recurrencia del cáncer de mama después de recibir la terapia de mantenimiento CM. Basándose en este hallazgo, Rusakiewicz S et al. caracterizaron las características de infiltración de células inmunitarias en pacientes con TNBC mediante tecnología de tinción de inmunofluorescencia 6-plex. Evaluaron el valor pronóstico de subconjuntos específicos de células inmunitarias y su papel predictivo en la eficacia de la terapia de mantenimiento CM, al tiempo que analizaron el impacto de las características de distribución espacial de las células inmunitarias en la eficacia del tratamiento y el pronóstico de los pacientes. Este estudio proporciona una base para formular estrategias de tratamiento precisas para pacientes con TNBC.
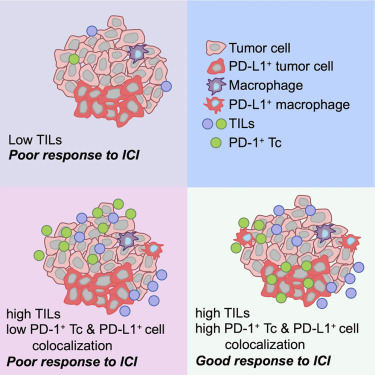
Compartir Literatura: Inmunofluorescencia Múltiple para la Predicción de la Eficacia Terapéutica de ICI en el Cáncer de Mama Temprano
En los últimos años, los inhibidores de puntos de control inmunológico (ICIs) han demostrado un valor potencial en el tratamiento del cáncer de mama, pero las respuestas al tratamiento varían significativamente entre diferentes pacientes. Las características del microambiente inmunológico tumoral (TIME) son factores clave que afectan la eficacia de los ICIs. Actualmente, todavía falta una definición sistemática y precisa de los biomarcadores predictivos de la respuesta al tratamiento con inhibidores de PD-L1 en pacientes con cáncer de mama, especialmente las diferencias en los mecanismos de respuesta al tratamiento entre diferentes subtipos receptores de cáncer de mama no se han elucidado completamente. Las nuevas tecnologías de detección desarrolladas en los últimos años pueden evaluar múltiples marcadores simultáneamente mientras preservan completamente las relaciones espaciales de las células in situ, y se están aplicando ampliamente a la caracterización del microambiente inmunológico tumoral y la minería de biomarcadores inmunológicos relacionados. Entre ellas, la tecnología de inmunofluorescencia múltiple (mIF) ha demostrado valor de aplicación en la predicción de la eficacia de los ICIs en varios tumores, superando significativamente las firmas de expresión génica, la carga mutacional tumoral y la detección estandarizada de PD-L1 por inmunohistoquímica.
Factor de Transcripción GATA
Las proteínas GATA comprenden un grupo de factores de transcripción relacionados por la presencia de dominios de unión al ADN de dedo de zinc conservados, que se unen directamente al elemento central de secuencia nucleotídica GATA. Existen seis proteínas GATA vertebradas, designadas GATA-1 a GATA-6. Aunque comúnmente se dividen en factores hematopoyéticos (GATA-1-3) o cardíacos (GATA-4-6), las proteínas GATA se expresan en una amplia variedad de tejidos y desempeñan roles críticos en el desarrollo embrionario y la diferenciación orgánica.