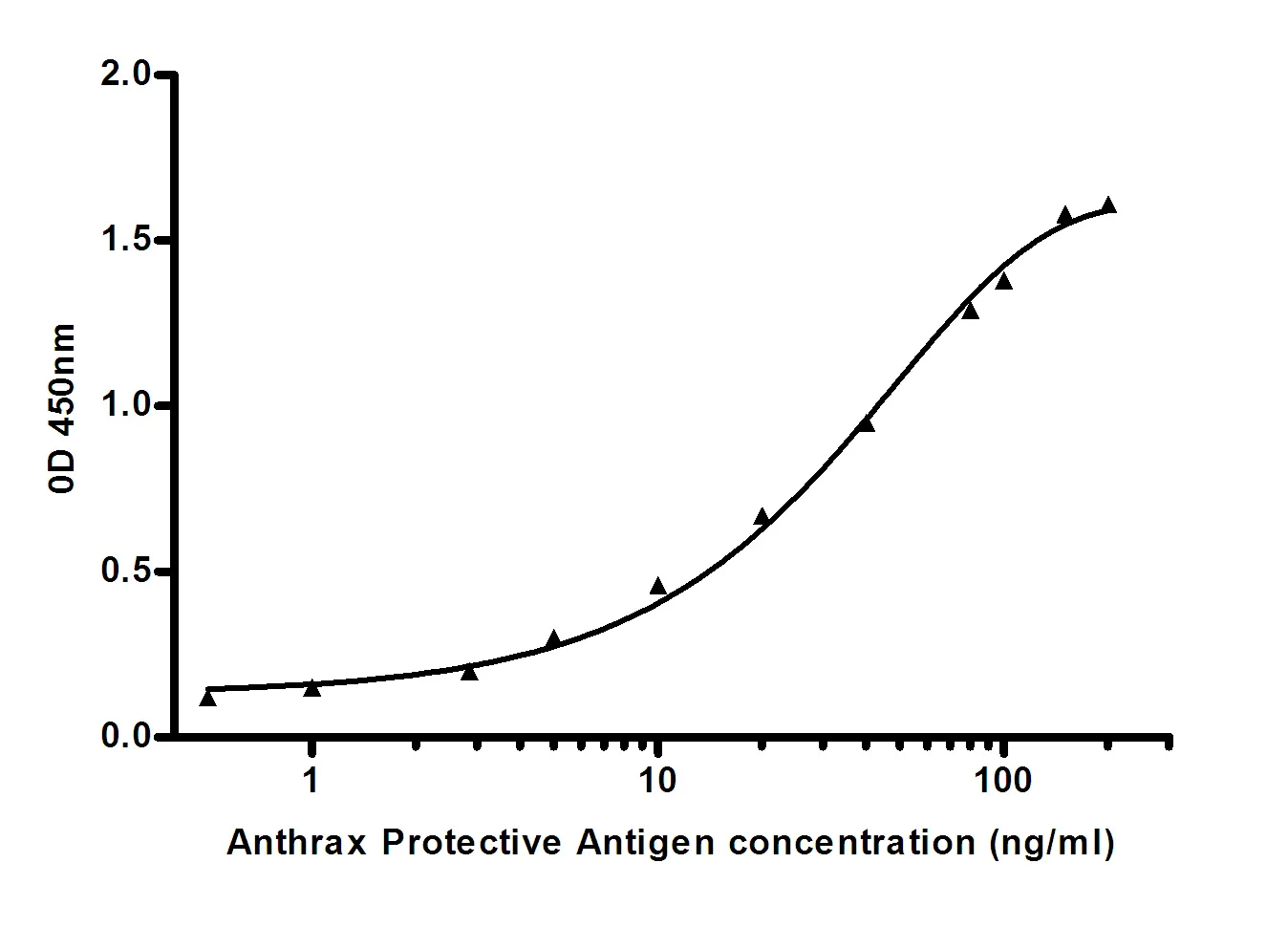
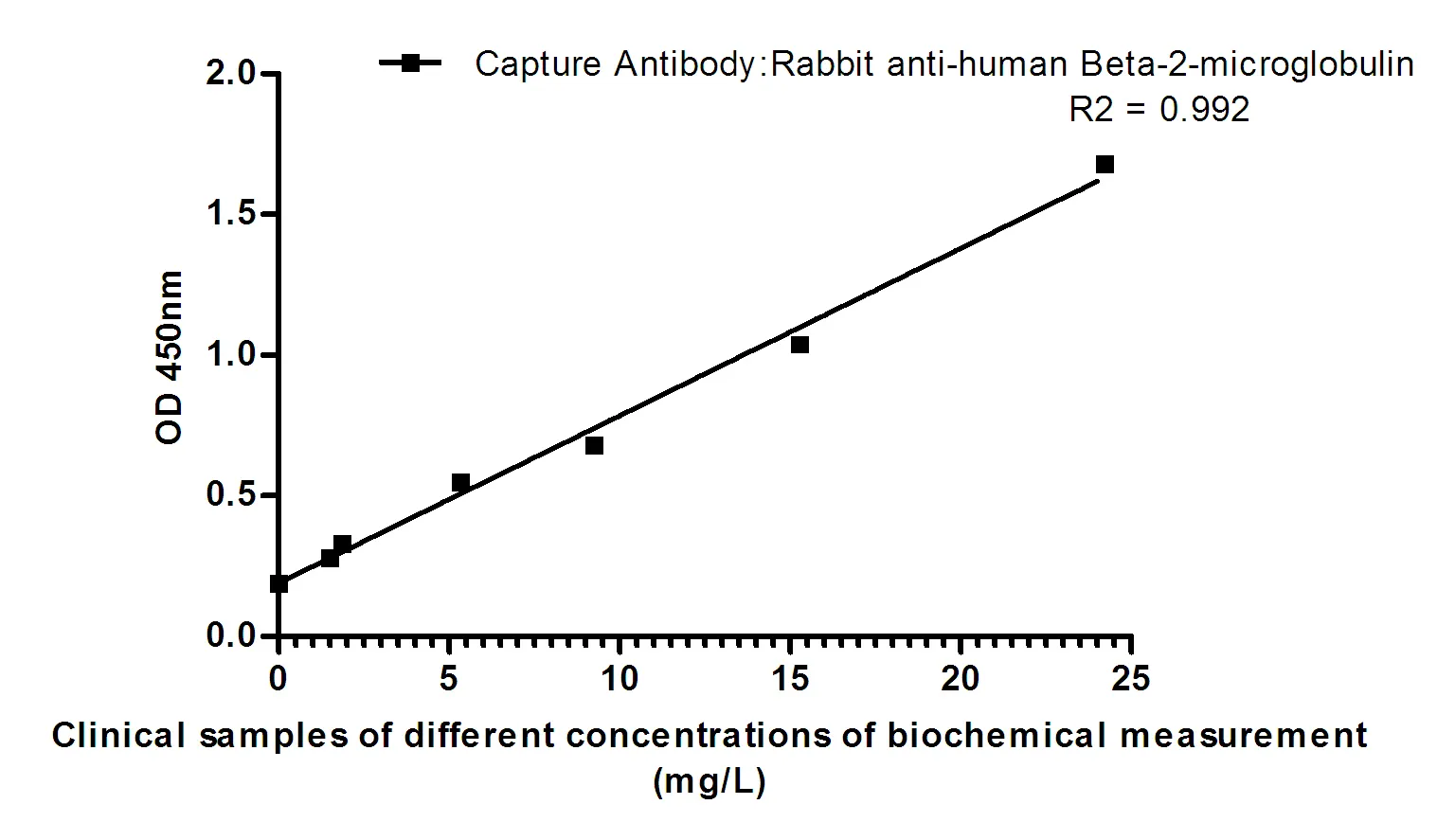
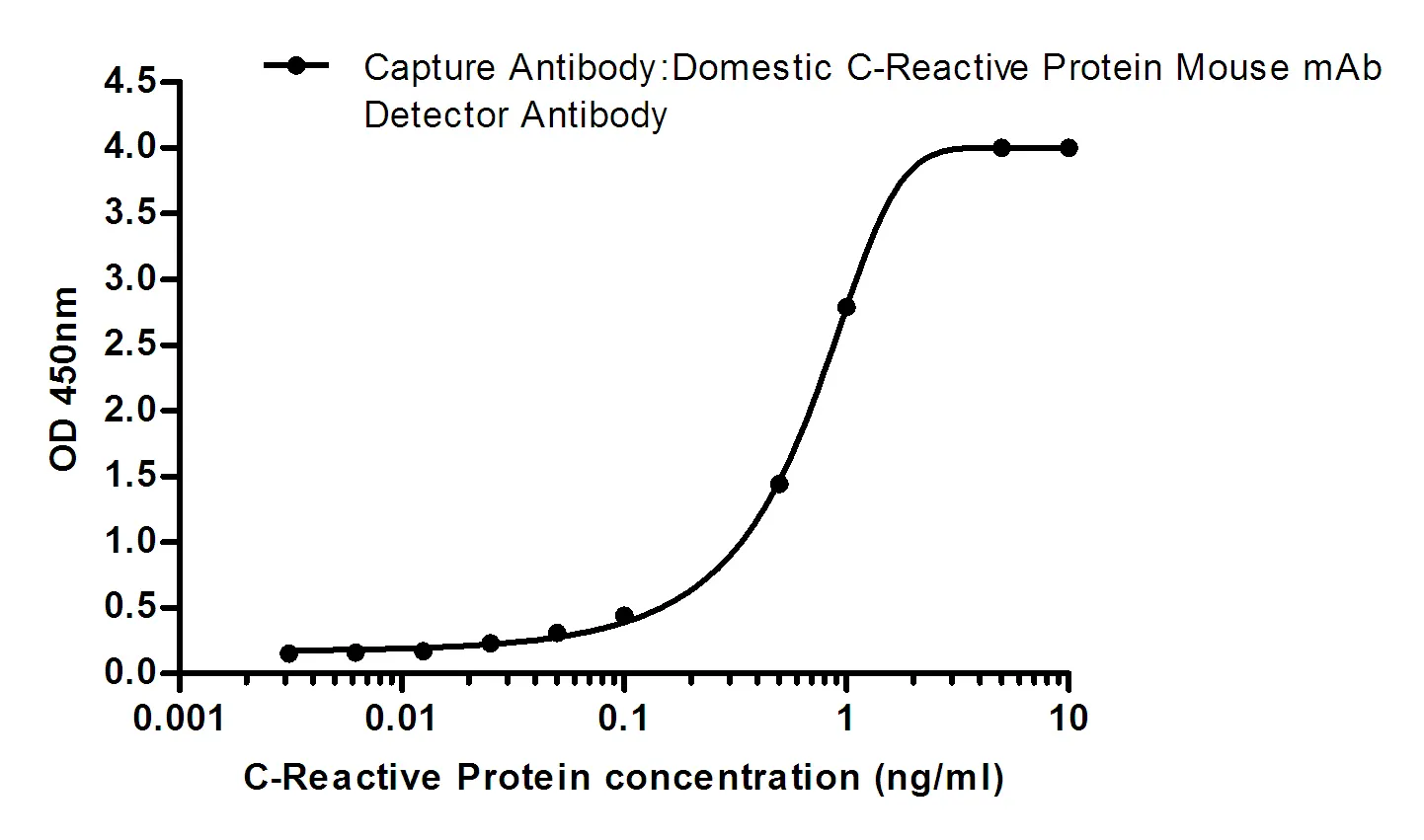
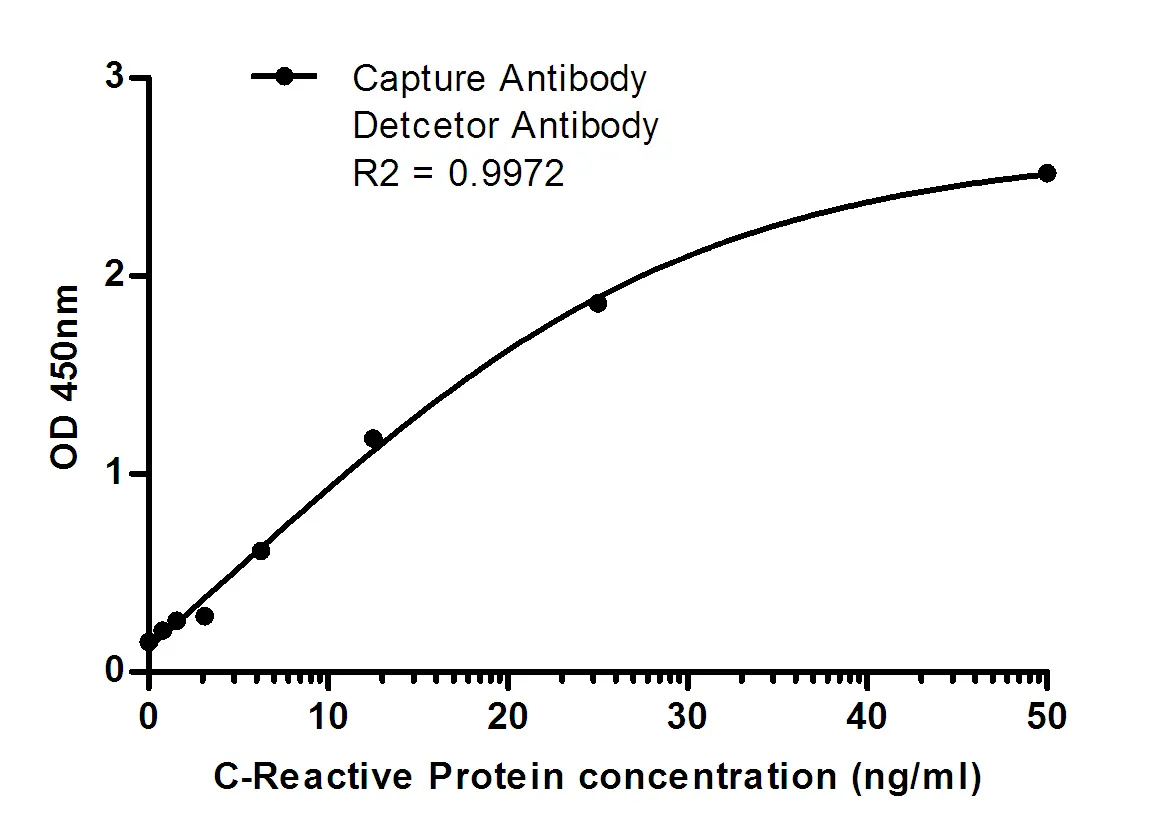
Anticuerpo monoclonal de ratón 2(PMS2)(PT2116) con aumento de la segregación posmeiótica
Conjugación: No conjugado
Anticuerpo monoclonal de ratón
Aplicación
Reactividad
Humano, Ratón
Nombre del gen
PMS2 PMSL2
Almacenamiento
Alicuotar y almacenar a -20 °C (válido por 12 meses). Evitar ciclos de congelación y descongelación.
Resumen
| Nombre del producto | Anticuerpo monoclonal de ratón 2(PMS2)(PT2116) con aumento de la segregación posmeiótica |
| Descripción | Anticuerpo monoclonal de ratón |
| Hospedador | Ratón |
| Reactividad | Humano, Ratón |
| Conjugación | No conjugado |
| Modificación | Sin modificar |
| isotipo | IgG |
| Clonalidad | Monoclonal |
| Forma | Líquido |
| Concentración | No conjugado |
| Almacenamiento | Alicuotar y almacenar a -20 °C (válido por 12 meses). Evitar ciclos de congelación y descongelación. |
| Envío | Bolsas de hielo. |
| Buffer | Líquido en PBS que contiene 50% de glicerol, 0,5% de proteína protectora y 0,02% de conservante de nuevo tipo N. |
| Purificación | Purificación por afinidad |
Información del antígeno
| Nombre del gen | PMS2 PMSL2 |
| Nombres alternativos | Mismatch repair endonuclease PMS2 (EC 3.1.-.-;DNA mismatch repair protein PMS2;PMS1 protein homolog 2) |
| Gene ID | 5395 |
| SwissProt ID | P54278 |
| Immunogen | Péptido sintetizado derivado de la segregación postmeiótica aumentada 2(PMS2) humana. Rango de AA: 600-700 |
Aplicación
| Aplicación | WB,IHC |
| Proporción de dilución | WB 1:200-1:1000,IHC 1:200-1:400 |
| Peso molecular | - |
Área de investigación
| Epigenetics and Nuclear Signaling; DNA / RNA; DNA Damage & Repair; Mismatch Repair |
Antecedentes
| Enfermedad: Los defectos en PMS2 son causa del síndrome de cáncer por reparación de desajustes (MMRCS) [MIM:276300]; también conocido como síndrome de Turcot y síndrome de tumor cerebral-poliposis 1 (BTPS1). El MMRCS es un trastorno autosómico dominante caracterizado por tumores malignos cerebrales asociados a múltiples adenomas colorrectales. Las características cutáneas incluyen quistes sebáceos, hiperpigmentación y manchas café con leche. Enfermedad: Los defectos en PMS2 son causa del cáncer colorrectal hereditario sin poliposis tipo 4 (HNPCC4) [MIM:600259]. Las mutaciones en más de un locus genético pueden estar implicadas, solas o en combinación, en la producción del fenotipo HNPCC (también llamado síndrome de Lynch). La mayoría de las familias con HNPCC clínicamente reconocido presentan mutaciones en los genes MLH1 o MSH2. El HNPCC es una enfermedad autosómica de herencia dominante asociada con un marcado aumento de la susceptibilidad al cáncer. Se caracteriza por una predisposición familiar al carcinoma colorrectal de aparición temprana (CCR) y cánceres extracolónicos de los tractos gastrointestinal, urológico y reproductivo femenino. Se informa que el HNPCC es la forma más común de cáncer colorrectal hereditario en el mundo occidental y representa el 15% de todos los cánceres de colon. Los cánceres en el HNPCC se originan dentro de pólipos neoplásicos benignos denominados adenomas. Clínicamente, el HNPCC a menudo se divide en dos subgrupos. Tipo I: predisposición hereditaria al cáncer colorrectal, una edad temprana de inicio y carcinoma observado en el colon proximal. Tipo II: los pacientes tienen un mayor riesgo de cánceres en ciertos tejidos como el útero, el ovario, la mama, el estómago, el intestino delgado, la piel y la laringe, además del colon. El diagnóstico del HNPCC clásico se basa en los criterios de Ámsterdam: 3 o más familiares afectados por cáncer colorrectal, uno familiar de primer grado de los otros dos; 2 o más generaciones afectadas; Uno o más cánceres colorrectales que se presentan antes de los 50 años; se excluyen los síndromes de poliposis hereditaria. El término "sospecha de HNPCC" o "HNPCC incompleto" puede utilizarse para describir a familias que no cumplen o solo cumplen parcialmente los criterios de Ámsterdam, pero en quienes se sospecha firmemente una base genética para el cáncer de colon. Función: Componente del sistema de reparación de desajustes del ADN (MMR) posreplicativo. Heterodimeriza con MLH1 para formar MutL alfa. La reparación del ADN se inicia mediante la unión de MutS alfa (MSH2-MSH6) o MutS beta (MSH2-MSH6) a un desajuste de ADN bicatenario, tras lo cual MutL alfa se recluta al heterodúplex. El ensamblaje del complejo ternario MutL-MutS-heterodúplex en presencia de RFC y PCNA es suficiente para activar la actividad endonucleasa de PMS2. Introduce roturas de cadena sencilla cerca del desajuste y, por lo tanto, genera nuevos puntos de entrada para que la exonucleasa EXO1 degrade la cadena que contiene el desajuste. La metilación del ADN evitaría la escisión y, por lo tanto, aseguraría que solo se corrija la cadena de ADN recién mutada. MulL alfa (MLH1-PMS2) interactúa físicamente con las subunidades del cargador de la ADN polimerasa III, lo que sugiere que puede desempeñar un papel en el reclutamiento de la ADN polimerasa III al sitio del MMR. También está implicada en la señalización del daño del ADN, un proceso que induce la detención del ciclo celular y puede conducir a la apoptosis en caso de daños importantes en el ADN. Similitud: Pertenece a la familia mutL/hexB de reparación de desajustes del ADN. Subunidad: Heterodímero de PMS2 y MLH1 (MutL alfa). Forma un complejo ternario con MutS alfa (MSH2-MSH6) o MutS beta (MSH2-MSH3). Parte del complejo de vigilancia genómica asociado a BRCA1 (BASC), que contiene BRCA1, MSH2, MSH6, MLH1, ATM, BLM, PMS2 y el complejo proteico RAD50-MRE11-NBS1. Esta asociación podría ser un proceso dinámico que cambia a lo largo del ciclo celular y dentro de los dominios subnucleares. |