Anticuerpo monoclonal de ratón HSPA5
Conjugación: No conjugado
Anticuerpo monoclonal de ratón
Aplicación
Reactividad
Humano, Ratón, Rata, Mono, Conejo
Nombre del gen
HSPA5
Almacenamiento
Alicuotar y almacenar a -20 °C (válido por 12 meses). Evitar ciclos de congelación y descongelación.
Resumen
| Nombre del producto | Anticuerpo monoclonal de ratón HSPA5 |
| Descripción | Anticuerpo monoclonal de ratón |
| Hospedador | Ratón |
| Reactividad | Humano, Ratón, Rata, Mono, Conejo |
| Conjugación | No conjugado |
| Modificación | Sin modificar |
| isotipo | Mouse IgG1 |
| Clonalidad | Monoclonal |
| Forma | Líquido |
| Concentración | No conjugado |
| Almacenamiento | Alicuotar y almacenar a -20 °C (válido por 12 meses). Evitar ciclos de congelación y descongelación. |
| Envío | Bolsas de hielo. |
| Buffer | Anticuerpo purificado en PBS con azida sódica al 0,05%. |
| Purificación | Purificación por afinidad |
Información del antígeno
| Nombre del gen | HSPA5 |
| Nombres alternativos | BIP; MIF2; GRP78; FLJ26106; HSPA5 |
| Gene ID | 3309 |
| SwissProt ID | P11021 |
| Immunogen | Fragmento recombinante purificado de HSPA5 humana expresado en E. Coli. |
Aplicación
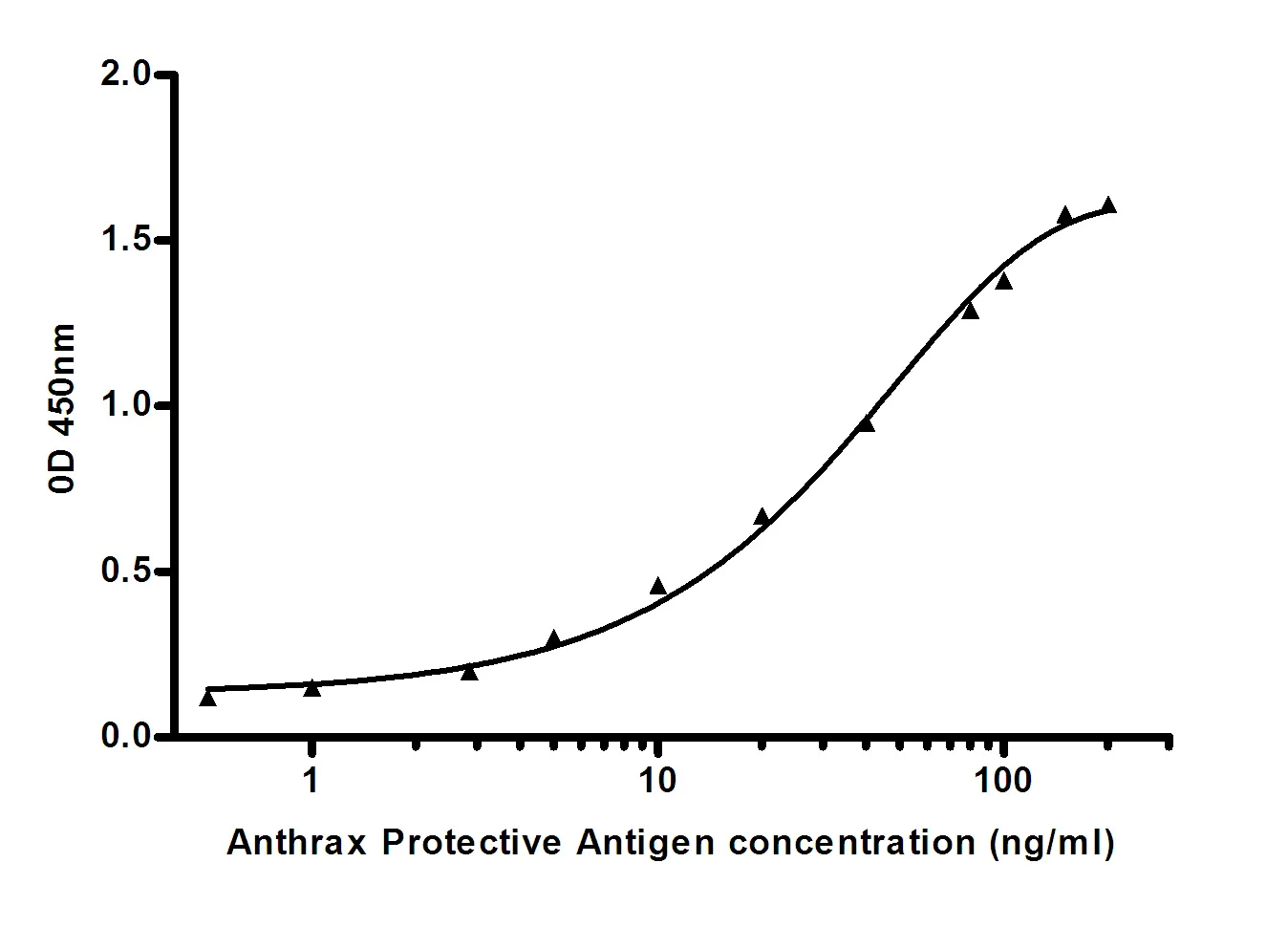
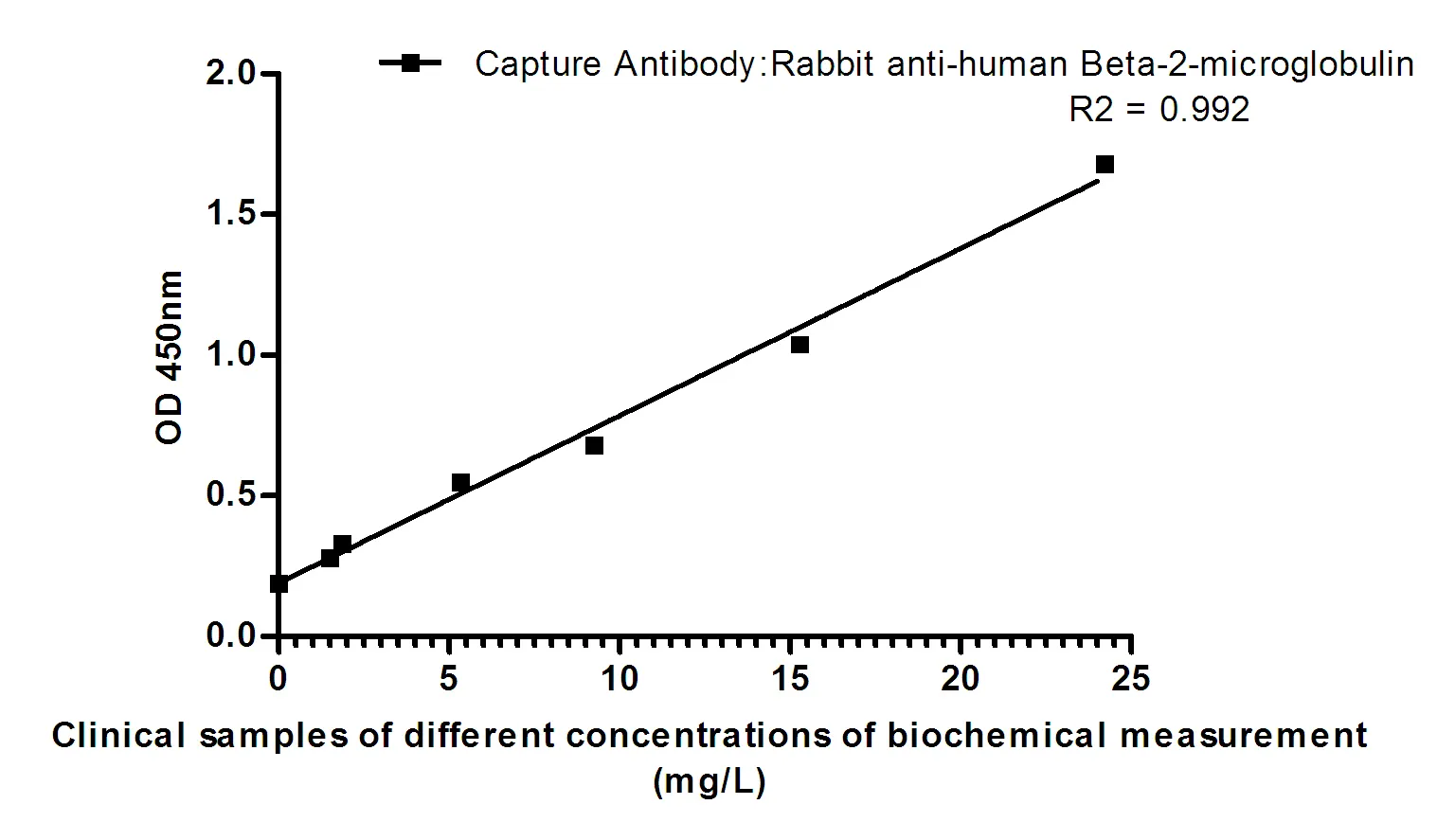
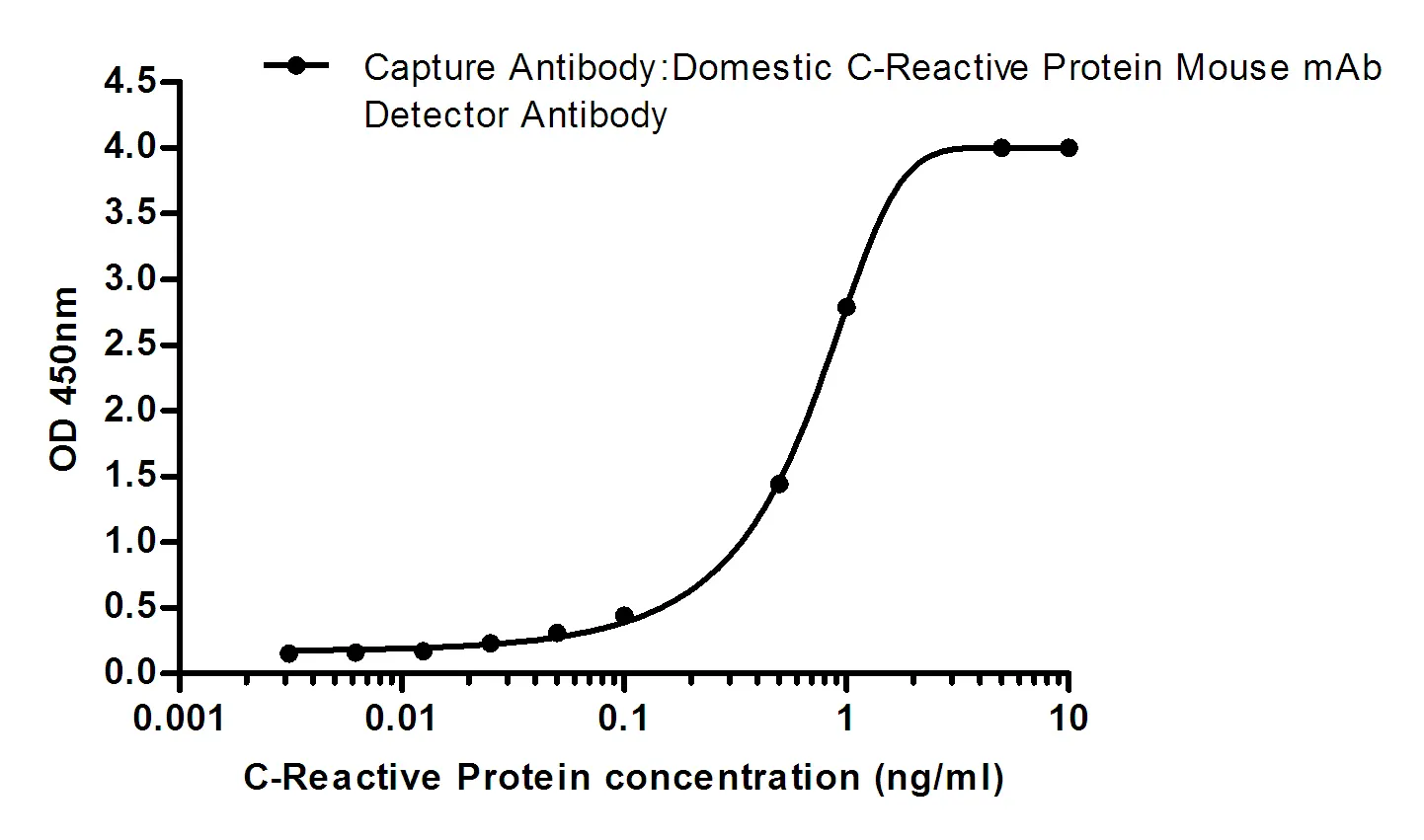
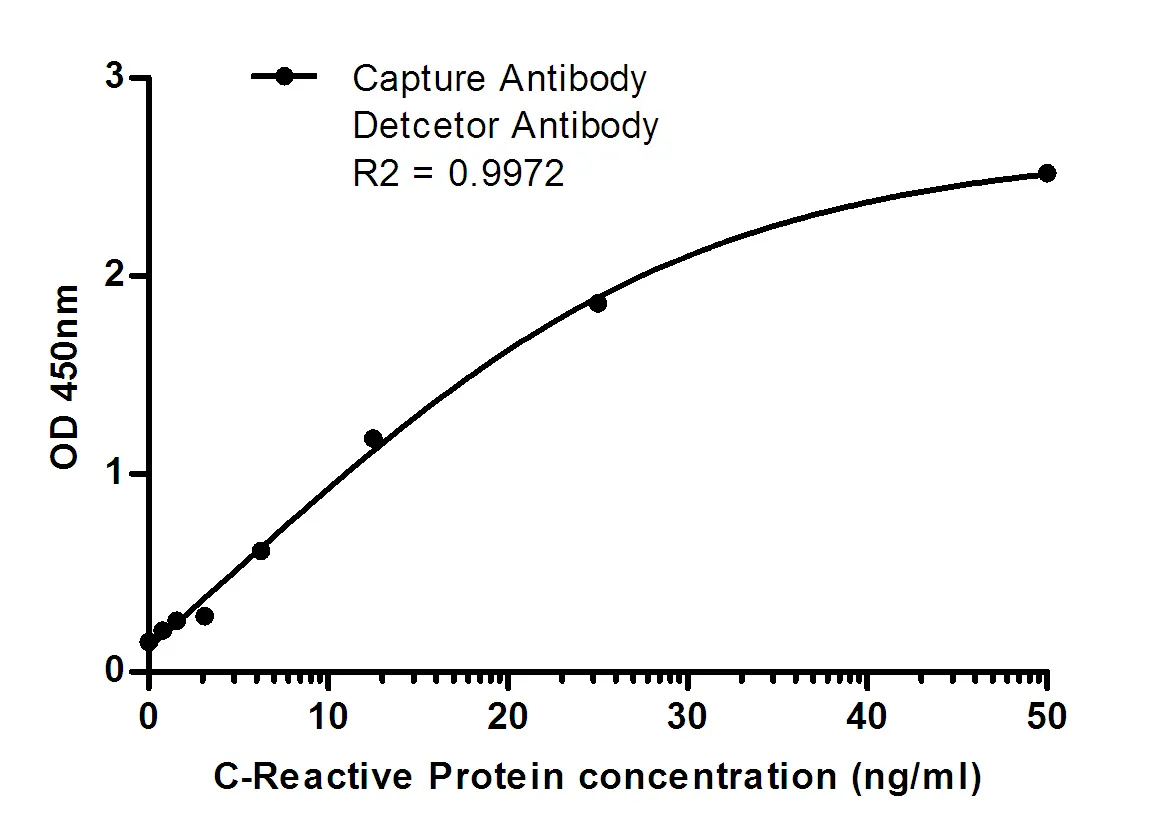
| Aplicación | WB,IHC,ICC,ELISA,FC |
| Proporción de dilución | WB 1:500-1:2000,IHC 1:100-1:500,ICC 1:50-1:500,ELISA 1:5000-1:20000,FC 1:200-1:400 |
| Peso molecular | 78kDa |
Área de investigación
Antecedentes
| Cuando las células K12 de hámster chino se ven privadas de glucosa, la síntesis de varias proteínas, llamadas proteínas reguladas por glucosa (GRP), aumenta notablemente. Hendershot et al. (1994) (PubMed 8020977) señalaron que una de estas, GRP78 (HSPA5), también conocida como "proteína de unión a la cadena pesada de inmunoglobulina" (BiP), pertenece a la familia de las proteínas de choque térmico 70 (HSP70) y participa en el plegamiento y ensamblaje de proteínas en el retículo endoplasmático (RE). Debido a que muchas proteínas del RE interactúan transitoriamente con GRP78, esta podría desempeñar un papel clave en la monitorización del transporte de proteínas a través de la célula. Probablemente, facilita el ensamblaje de complejos proteicos multiméricos dentro del RE. Las proteínas HSP70 son chaparonas moleculares ubicuas que se encuentran en todos los organismos y tipos de tejidos. Al igual que otros miembros de la familia HSP70, BiP es una ATPasa de unión a péptidos capaz de diferenciar proteínas nativas de polipéptidos desdoblados. BiP no se une a proteínas completamente plegadas y ensambladas, excepto en presencia de otras cochaparonas. BiP participa en diversos mecanismos y vías clave, como la translocación de polipéptidos a través del retículo endoplasmático, el plegamiento, el ensamblaje, el transporte de proteínas secretadas o de membrana, y la regulación de la homeostasis del calcio. Aunque BiP es relativamente abundante, se producen aumentos marcados de BiP donde hay acumulación de polipéptidos desdoblados. Por esta razón, BiP se ha identificado como un marcador de diversas enfermedades asociadas con el plegamiento incorrecto de proteínas secretoras y transmembrana. |