Anticuerpo monoclonal de conejo FAP1 (17O11)
Conjugación: No conjugado
Anticuerpo monoclonal de conejo recombinante
Aplicación
Reactividad
Humano, Ratón
Nombre del gen
FAP
Almacenamiento
Alicuotar y almacenar a -20 °C (válido por 12 meses). Evitar ciclos de congelación y descongelación.
Resumen
| Nombre del producto | Anticuerpo monoclonal de conejo FAP1 (17O11) |
| Descripción | Anticuerpo monoclonal de conejo recombinante |
| Hospedador | Conejo |
| Reactividad | Humano, Ratón |
| Conjugación | No conjugado |
| Modificación | Sin modificar |
| isotipo | IgG |
| Clonalidad | Monoclonal |
| Forma | Líquido |
| Concentración | No conjugado |
| Almacenamiento | Alicuotar y almacenar a -20 °C (válido por 12 meses). Evitar ciclos de congelación y descongelación. |
| Envío | Bolsas de hielo. |
| Buffer | IgG de conejo en solución salina tamponada con fosfato, pH 7,4, 150 mM de NaCl, 0,02 % de conservante de nuevo tipo N y 50 % de glicerol. Conservar a +4 °C a corto plazo. Conservar a -20 °C a largo plazo. Evitar el ciclo de congelación/descongelación. |
| Purificación | Purificación por afinidad |
Información del antígeno
| Nombre del gen | FAP |
| Nombres alternativos | 170 kDa melanoma membrane bound gelatinase; DPPIV; FAP; FAPA; Seprase; |
| Gene ID | 2191 |
| SwissProt ID | Q12884 |
| Immunogen | Proteína recombinante de la proteína de activación de fibroblastos humanos, alfa |
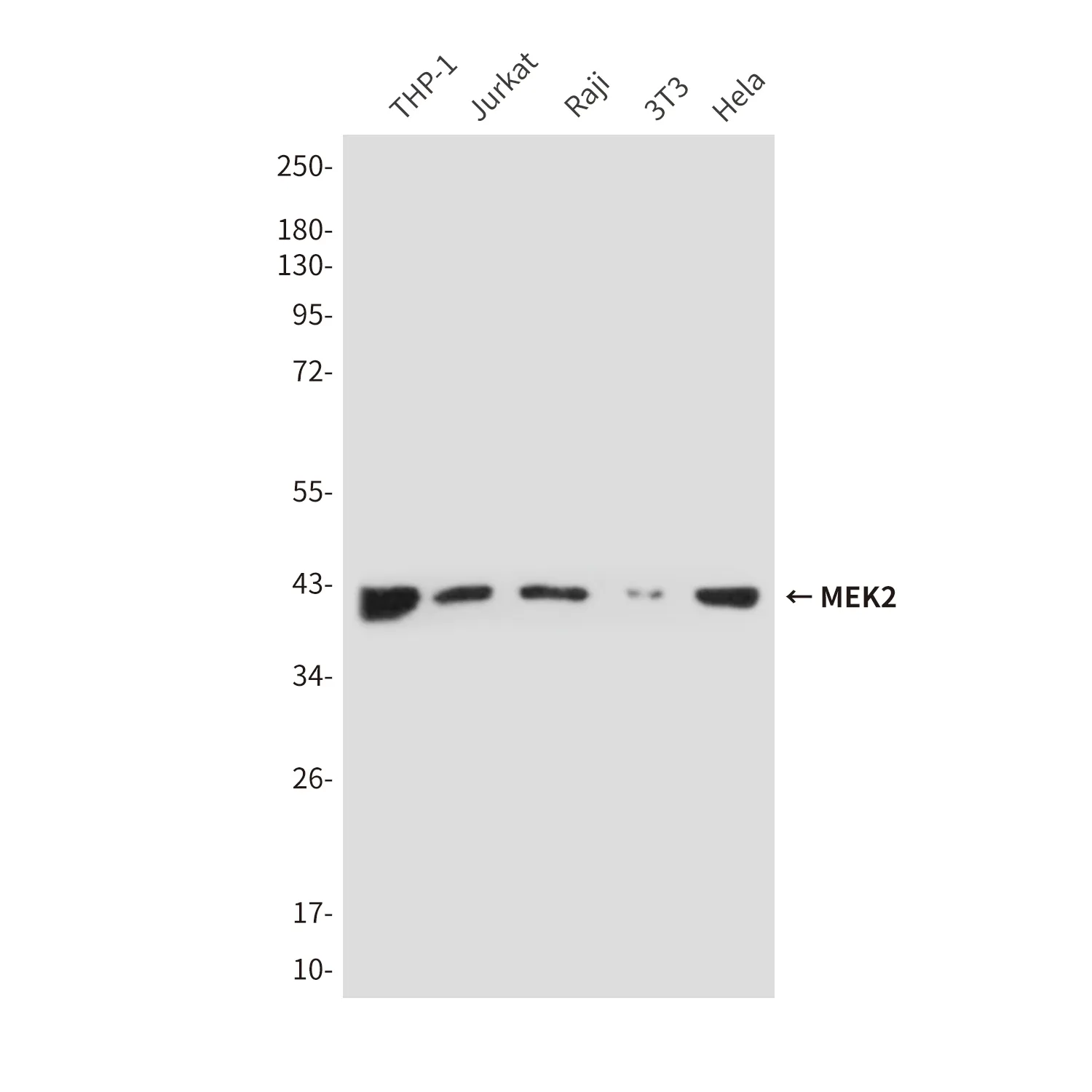
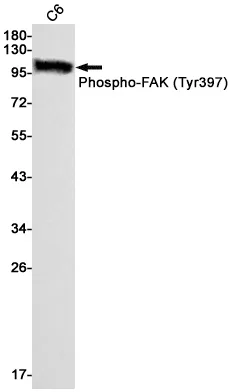
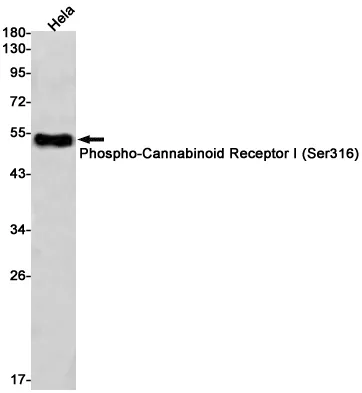
Aplicación
| Aplicación | WB,IHC,IF-P |
| Proporción de dilución | WB 1:500-1:2000,IHC 1:100-1:200,IF-P 1:100-1:200 |
| Peso molecular | 88kDa |
Área de investigación
| Cell Biology |
Antecedentes
| En asociación con la DPP4, participa en la proteólisis pericelular de la matriz extracelular (MEC), la migración e invasión de células endoteliales hacia la MEC. Puede desempeñar un papel en la remodelación tisular durante el desarrollo y la cicatrización de heridas, y puede contribuir a la invasividad en cánceres malignos. La glicoproteína serina proteasa de superficie celular participa en la degradación de la matriz extracelular y participa en numerosos procesos celulares, como la remodelación tisular, la fibrosis, la cicatrización de heridas, la inflamación y el crecimiento tumoral. Tanto las formas de membrana plasmática como las solubles exhiben actividad endopeptidasa de escisión posterior a la prolina, con una marcada preferencia por las secuencias de consenso Ala/Ser-Gly-Pro-Ser/Asn/Ala, en sustratos como la alfa-2-antiplasmina SERPINF2 y SPRY2 (PubMed:14751930, PubMed:16223769, PubMed:16480718, PubMed:16410248, PubMed:17381073, PubMed:18095711, PubMed:21288888, PubMed:24371721). También degradan la gelatina, el colágeno tipo I desnaturalizado por calor, pero no el colágeno nativo tipo I y IV, la vitronectina, la tenascina, la laminina, la fibronectina, la fibrina o la caseína (PubMed:9065413, PubMed:2172980, PubMed:7923219, PubMed:10347120, PubMed:10455171, PubMed:12376466, PubMed:16223769, PubMed:16651416, PubMed:18095711). También tiene actividad de dipeptidil peptidasa, exhibiendo la capacidad de hidrolizar el enlace prolilo dos residuos del extremo N de sustratos dipeptídicos sintéticos, siempre que el penúltimo residuo sea prolina, con preferencia por Ala-Pro, Ile-Pro, Gly-Pro, Arg-Pro y Pro-Pro (PubMed:10347120, PubMed:10593948, PubMed:16175601, PubMed:16223769, PubMed:16651416, PubMed:16410248, PubMed:17381073, PubMed:21314817, PubMed:24371721, PubMed:24717288). Las hormonas neuropeptídicas naturales para la dipeptidil peptidasa son el neuropéptido Y (NPY), el péptido YY (PYY), la sustancia P (TAC1) y el péptido natriurético cerebral 32 (NPPB) (PubMed:21314817). La forma de membrana plasmática, en asociación con DPP4, PLAUR o integrinas, participa en la proteólisis pericelular de la matriz extracelular (MEC) y, por lo tanto, promueve la adhesión celular, la migración y la invasión a través de la MEC. Desempeña un papel en la remodelación tisular durante el desarrollo y la cicatrización de heridas. Participa en la invasividad celular hacia la MEC en cánceres de melanoma malignos. Mejora la progresión del crecimiento tumoral al aumentar la angiogénesis, la degradación de las fibras de colágeno y la apoptosis, y al reducir la respuesta antitumoral del sistema inmunitario. Promueve la invasión de células de glioma a través del parénquima cerebral al degradar el proteoglicano brevicano. Actúa como supresor de tumores en células melanocíticas mediante la regulación de la proliferación y supervivencia celular de una manera independiente de la actividad de la serina proteasa. |