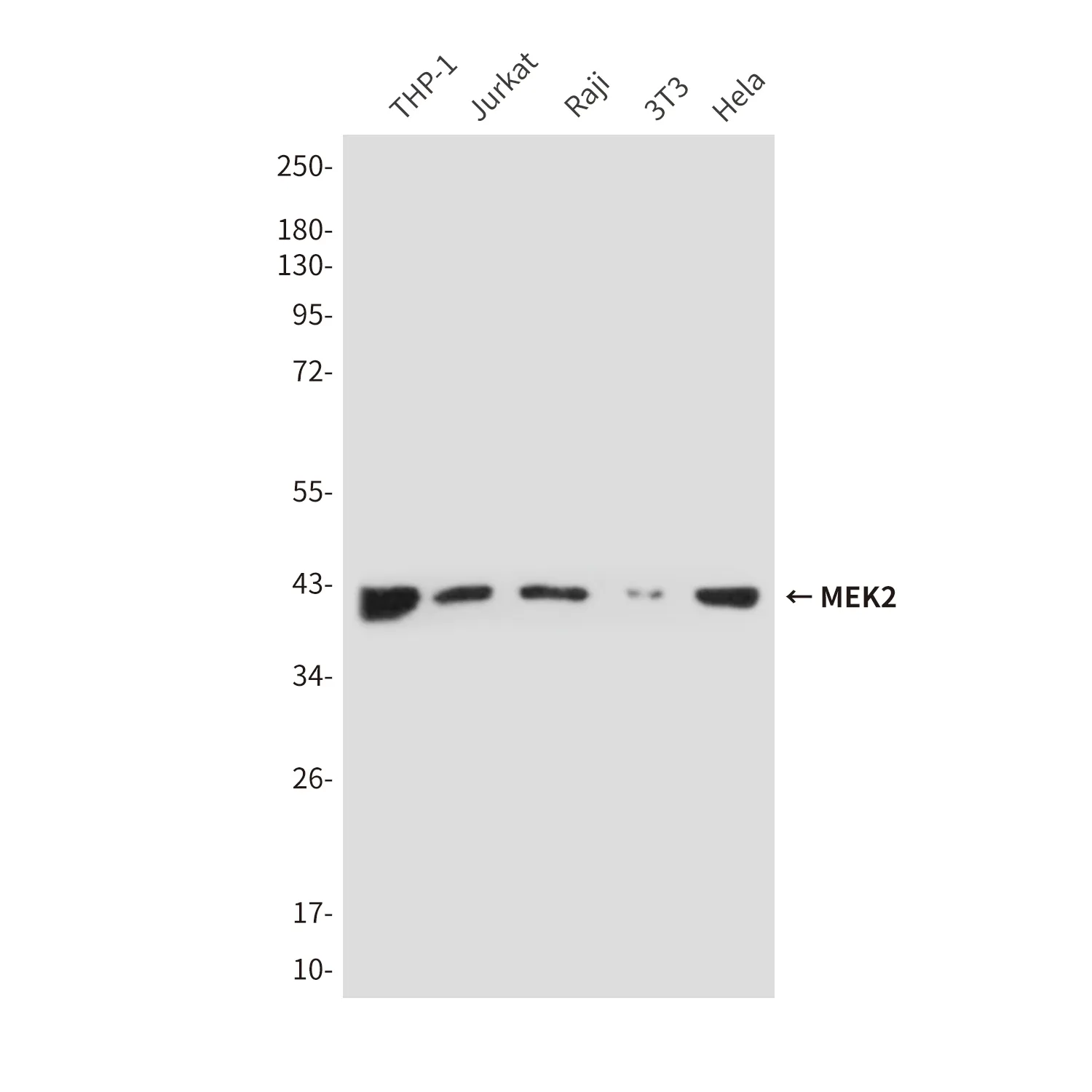
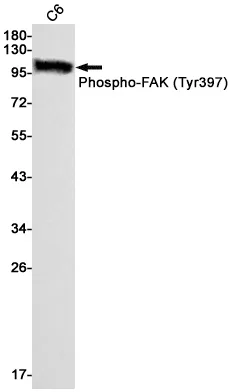
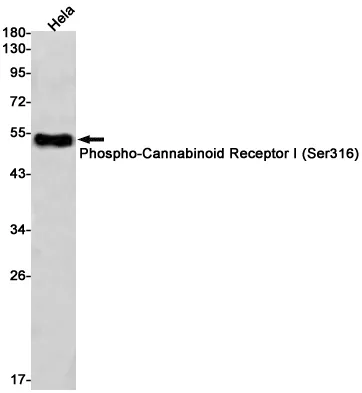
Anticuerpo monoclonal de conejo citocromo P450 1A2 (8B7)
Conjugación: No conjugado
Anticuerpo monoclonal de conejo recombinante
Aplicación
Reactividad
Humano
Nombre del gen
CYP1A2
Almacenamiento
Alicuotar y almacenar a -20 °C (válido por 12 meses). Evitar ciclos de congelación y descongelación.
Resumen
| Nombre del producto | Anticuerpo monoclonal de conejo citocromo P450 1A2 (8B7) |
| Descripción | Anticuerpo monoclonal de conejo recombinante |
| Hospedador | Conejo |
| Reactividad | Humano |
| Conjugación | No conjugado |
| Modificación | Sin modificar |
| isotipo | IgG |
| Clonalidad | Monoclonal |
| Forma | Líquido |
| Concentración | No conjugado |
| Almacenamiento | Alicuotar y almacenar a -20 °C (válido por 12 meses). Evitar ciclos de congelación y descongelación. |
| Envío | Bolsas de hielo. |
| Buffer | IgG de conejo en solución salina tamponada con fosfato, pH 7,4, 150 mM de NaCl, 0,02 % de conservante de nuevo tipo N y 50 % de glicerol. Conservar a +4 °C a corto plazo. Conservar a -20 °C a largo plazo. Evitar el ciclo de congelación/descongelación. |
| Purificación | Purificación por afinidad |
Información del antígeno
| Nombre del gen | CYP1A2 |
| Nombres alternativos | CP12; CYP1A2; CYPIA2; P3 450; P450 4; P450 P3; |
| Gene ID | 1544 |
| SwissProt ID | P05177 |
| Immunogen | Un péptido sintético del citocromo P450 1A2 humano |
Aplicación
| Aplicación | WB,ICC/IF,FC |
| Proporción de dilución | WB 1:1000-1:5000,ICC/IF 1:200-1:500,FC 1:50-1:200 |
| Peso molecular | 58kDa |
Área de investigación
| Caffeine metabolism;Tryptophan metabolism;Linoleic acid metabolism;Retinol metabolism;Metabolism of xenobiotics by cytochrome P450;Drug metabolism; |
Antecedentes
| Los citocromos P450 son un grupo de hemotiolato monooxigenasas. En los microsomas hepáticos, esta enzima participa en una vía de transporte de electrones dependiente de NADPH. Una citocromo P450 monooxigenasa participa en el metabolismo de diversos sustratos endógenos, como ácidos grasos, hormonas esteroides y vitaminas (PubMed:9435160, PubMed:10681376, PubMed:11555828, PubMed:12865317, PubMed:19965576). Mecanísticamente, utiliza oxígeno molecular insertando un átomo de oxígeno en un sustrato y reduciendo el segundo en una molécula de agua, con dos electrones proporcionados por NADPH a través de la citocromo P450 reductasa (NADPH--hemoproteína reductasa) (PubMed:9435160, PubMed:10681376, PubMed:11555828, PubMed:12865317, PubMed:19965576). Cataliza la hidroxilación de enlaces carbono-hidrógeno (PubMed:11555828, PubMed:12865317). Exhibe alta actividad catalítica para la formación de hidroxiestrógenos a partir de estrona (E1) y 17beta-estradiol (E2), a saber, 2-hidroxi E1 y E2 (PubMed:11555828, PubMed:12865317). Metaboliza el colesterol a 25-hidroxicolesterol, un regulador fisiológico de la homeostasis celular del colesterol (PubMed:21576599). Puede actuar como una enzima importante para la biosíntesis hepática del ácido retinoico all-trans. Cataliza dos transformaciones oxidativas sucesivas del retinol all-trans a retinal all-trans y, posteriormente, a la forma activa, el ácido retinoico all-trans (PubMed:10681376). Cataliza principalmente la epoxidación estereoselectiva del último doble enlace de los ácidos grasos poliinsaturados (PUFA), mostrando una marcada preferencia por el estereoisómero (R,S) (PubMed:19965576). Cataliza la hidroxilación bisalílica y la hidroxilación omega-1 de PUFA (PubMed:9435160). También puede participar en el metabolismo de los eicosanoides mediante la conversión de especies de hidroperóxido en metabolitos oxo (reacción similar a la lipooxigenasa, independiente del NADPH) (PubMed:21068195). Participa en el metabolismo oxidativo de xenobióticos. Cataliza la N-hidroxilación de aminas heterocíclicas y la O-desetilación de la fenacetina (PubMed:14725854). Metaboliza la cafeína mediante la N3-desmetilación (probable). |